【行研】化学原料药注册申报受理
扫一扫
分享文章到微信

扫一扫
关注豌豆财经网微信公众号
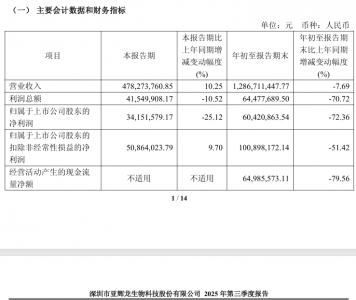
药品注册申报是药品全生命周期管理的重要组成部分,药品注册受理是药品申请人进行药品注册申报与官方监管建立链接的第一步。高效、规范地完成注册受理环节,不仅有助于缩短评审周期,也为后续审批审批工作的顺利开展奠定基础。本文梳理了化学原料药注册申报的受理程序、法规要求及常见注意事项,为原料药申报提供操作参考。
一、1.药品受理工作程序:
《中华人民共和国行政许可法》行政许可指行政机关根据公民、法人或者其他组织的申请,经依法审查,准予其从事特定活动的行为。行政许可的实施包括申请与受理、审查与决定等。国家药品监督管理局药品审评中心(CDE)对申请人递交的药品上市许可申请/原料药生产登记申请/药物临床试验申请等做出受理审查决定,受理审查决定包括不予受理、受理以及补正。对于申请材料齐全、符合法定形式、或提交全部补正申请材料的,且属于相关职权范围内的申请,官方予以受理。
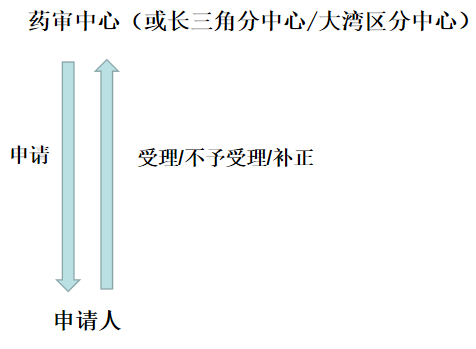
二、注册受理相关法规指南
近年来,国家药品监管部门陆续发布了多项具体指导原则,细化了各类注册申请的资料格式与内容要求,受理环节的规范性显著增强,要求更加公开透明。下方收集了原料药受理相关的指导原则,熟悉官方要求,是成功受理的第一步。
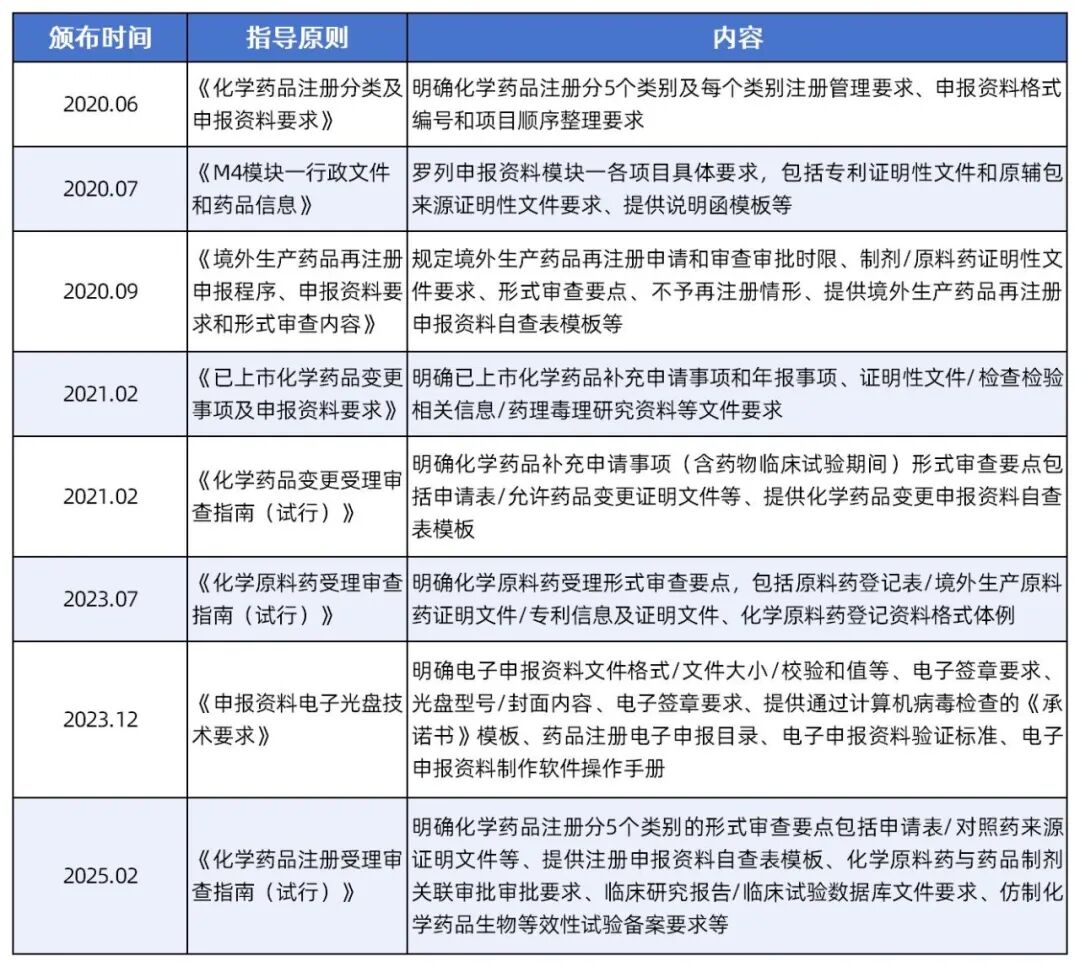
三、药品申报受理注意事项
国家药监局药审中心为了提高审评效率,明确受理要求,在中心网站上不定期公布受理共性问题,迄今为止,共计公布93个问题。通过提前学习和规避这些共性问题,申请人可以更有针对性地准备申报资料,从而大大提高首次提交的受理率,加速药品上市进程。
浙江九洲药业(603456)股份有限公司是一家以创新驱动发展的CDMO企业,长期为全球制药企业提供覆盖创新药临床前CMC研究、临床I–III期开发、NDA申报至商业化生产的一站式研发与注册服务。本文结合近年来在注册申报实践中的经验积累,以及对官方受理要求和培训要点的理解,就常见问题及注意事项进行简要分享,旨在帮助项目团队从源头规避可预防的申报障碍,提升注册效率。
投稿邮箱:lukejiwang@163.com 详情访问豌豆财经网:http://www.wdyxw.com.cn
 头条资讯
头条资讯